Diabète: l’Assurance maladie généralise son service Sophia
 Début 2013, Sophia franchit une étape décisive avec la généralisation du service à l’ensemble du territoire français. Ce sont désormais 1,8 millions de personnes diabétiques qui sont éligibles à ce service en santé innovant développé progressivement par l’Assurance Maladie depuis 2008. Sophia compte aujourd’hui 226 000 adhérents.
Début 2013, Sophia franchit une étape décisive avec la généralisation du service à l’ensemble du territoire français. Ce sont désormais 1,8 millions de personnes diabétiques qui sont éligibles à ce service en santé innovant développé progressivement par l’Assurance Maladie depuis 2008. Sophia compte aujourd’hui 226 000 adhérents.
L’objectif de ce service est d’accompagner de manière efficiente et personnalisée les patients diabétiques volontaires, en fonction de leur état d e santé et en relais du médecin traitant, afin de les aider à mieux vivre avec leur maladie et d’en prévenir les complications.
Alors que l’extension à tous les départements français est en cours, on compte aujourd’hui 226 000 adhérents et 55 800 médecins traitants concernés par le service . Dans les départements historiques dans lesquels sophia était proposé avant 2012, le taux d’adhésion atteint 34%, soit 1 patient éligible sur 3.
Après une 1 ère évaluation médico-économique menée en 2010, l’Assurance Maladie a actualisé cette étude afin de mesurer de manière régulière et à plus long terme les effets du service sophia. D’autres évaluations externes sont programmées pour les prochaines années.
Sur la période 2008-2011, les adhérents au service sophia voient le suivi de leur diabète s’améliorer sur la quasi-totalité des indicateurs mesurés : surveillance de l’équilibre glycémique, de la fonction rénale, examens ophtalmologiques réguliers,…
Si une amélioration est également observée, pour ce suivi des examens recommandés, dans la population témoin et dans la population non adhérente, la progression est significativement plus importante pour les adhérents lorsque l’on compare à profils de patients identiques. Les résultats à trois ans confirment donc l’évolution positive constatée un an après le lancement du service en 2009.
Des dépenses hospitalières moindres
Parallèlement, sur la période 2009-2011, les adhérents sophia ont, à caractéristiques égales, des dépenses de soins moins élevées que la population témoin , qu’il s’agisse des dépenses de soins de ville ou d’hospitalisation .
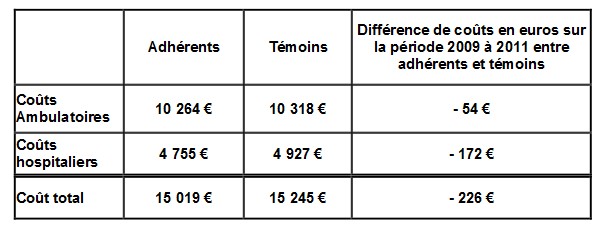
Si leurs dépenses hospitalières sont moindres, c’est notamment parce qu ’ils sont moins souvent hospitalisés pour leur diabète ou une de ses complications (complications cardio-vasculaires, rénales, plaies du pied,…). « Il s’agit là d’un résultat important, car l’objectif poursuivi par sophia, en soutenant les patients et en les aidant à mieux prendre en charge leur maladie chronique, est de contribuer à ralentir son aggravation. Les évaluations ultérieures montreront si ces résultats se confirment dans la durée », souligne la CNAMTS.
L’Assurance maladie a indiqué que l’année 2013 permettra un déploiement à grande échelle de sophia auprès des personnes diabétiques et également, d’ici la fin de l’année, d’étendre ce service aux personnes asthmatiques dans le cadre d’une expérimentation dans 18 départements français.
Source: Assurance maladie
