Industrie pharmaceutique : le Top 10 des sociétés les plus innovantes en 2017
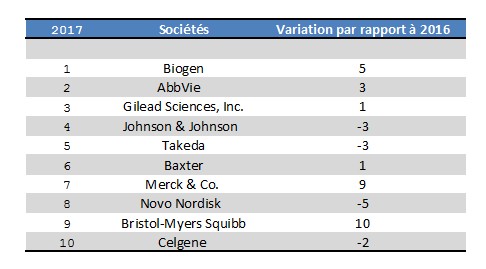
 Biogen décroche la 1ère place du palmarès 2017 de l’indice d’innovation productive (Pharmaceutical Innovation Index, PII*) d’IDEA Pharma, classant les entreprises pharmaceutiques selon leur capacité à mettre au point et à commercialiser avec succès de nouveaux médicaments. Abbvie et Gilead montent respectivement sur la 2ème et 3ème marche du podium.
Biogen décroche la 1ère place du palmarès 2017 de l’indice d’innovation productive (Pharmaceutical Innovation Index, PII*) d’IDEA Pharma, classant les entreprises pharmaceutiques selon leur capacité à mettre au point et à commercialiser avec succès de nouveaux médicaments. Abbvie et Gilead montent respectivement sur la 2ème et 3ème marche du podium.
« Après une analyse systématique et objective de la performance de chaque société entre 2011 et 2016, le classement 2017 voit le retour de certaines sociétés pharmaceutiques majeures parmi les Top 10, avec la forte augmentation de Bristol-Myers Squibb et Merck, et la performance solide continue des intervenants spécialisés de taille moyenne – Biogen se place en première position dans l’indice pour la première fois dans son histoire. Johnson & Johnson, qui a été en tête de l’Index pour 5 des 6 années précédentes, maintient une solide performance mais a été devancée par la performance exceptionnelle de Biogen, AbbVie et Gilead », commente Idea Pharma dans un communiqué.
« Le PII annuel est la vraie mesure de l’innovation dans l’industrie pharmaceutique – des médicaments significatifs avantageux pour les patients. La variation la plus saisissante dans les mesures R&D pour 2016 par rapport à l’année dernière était la baisse du nombre de nouveaux agents approuvés par la FDA : 22 pour 2016 contre 45 en 2015. Cependant, derrière ce gros titre étaient les sociétés qui ont obtenu les approbations : les surperformers des dernières années, GlaxoSmithKline (GSK), Johnson & Johnson (J&J) et Novartis, n’ont reçu aucune approbation de nouveau médicament en 2016. Amgen, AstraZeneca (AZ), Bayer et Bristol-Myers Squibb (BMS) non plus. Au total, sept des 13 grandes sociétés pharmaceutiques historiques, qui ont obtenu 14 approbations en 2015, sont restées les mains vides en 2016. Le fait que l’innovation est de plus en plus stimulée par des sociétés plus petites et potentiellement plus agiles a été mis en exergue par 14 des 22 approbations qu’elles ont obtenues. Il y a plusieurs signaux ici pour ceux qui sont prêts à écouter. Si l’on considère que « innovation » est un terme trop utilisé dans l’industrie à l’heure actuelle, le Pharmaceutical Innovation Index montre qui crée véritablement de la valeur pour les patients. », commente Mike Rea, PDG d’IDEA Pharma
*Le PII utilise des mesures subjectives de « l’innovation » et évalue les entreprises en fonction de divers facteurs parmi lesquels la rapidité de la commercialisation, le taux d’attrition à travers les phases – en particulier la phase III, les taux de remboursement, les approbations règlementaires, la performance sur le marché et les classements des analystes.
Pour voir plus en détail le Pharmaceutical Innovation Index et les 30 entreprises en tête de l’indice
Source : IDEA Pharma
