Le marché du selfcare en hausse de 4,8% en 2016
 L’Afipa (Association pour l’Automédication Responsable) vient de publier les résultats de son baromètre annuel, réalisé en collaboration avec OpenHealth Company*, qui présente un bilan chiffré du marché des médicaments d’automédication, dispositifs médicaux et compléments alimentaires. En 2016, le marché du selfcare progresse ainsi de 4,8% en valeur par rapport à 2015 (soit 3 883 M€).
L’Afipa (Association pour l’Automédication Responsable) vient de publier les résultats de son baromètre annuel, réalisé en collaboration avec OpenHealth Company*, qui présente un bilan chiffré du marché des médicaments d’automédication, dispositifs médicaux et compléments alimentaires. En 2016, le marché du selfcare progresse ainsi de 4,8% en valeur par rapport à 2015 (soit 3 883 M€).
« Cette année encore, le selfcare reste un pilier de la croissance de l’officine : il représente 10,7% du chiffre d’affaires des officines et contribue à 25% de leur croissance », indique l’Afipa dans un communiqué. D’ailleurs, l’épidémie de gastro-entérite de décembre 2016 a illustré le réflexe automédication des patients pour soigner leurs maux bénins : +21% de fréquentation dans les officines françaises pour le seul mois de décembre par rapport à la moyenne de l’année.
Selon le baromètre de l’Afipa, ce sont les dispositifs médicaux et compléments alimentaires qui boostent la dynamique du selfcare en 2016 avec une progression respective de 5%(soit 817 M€) et 9,3% (soit 736 M€). Pour autant, l’automédication ne connaît pas de croissance fulgurante en 2016 : +3,3%, soit 2 331 M€ par rapport à l’année 2015, et ce, malgré un niveau de prix bas : 4,74 euros en moyenne pour un médicament d’automédication.
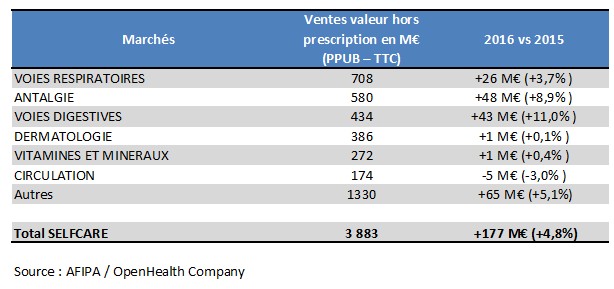
Classement sur les ventes valeur hors prescription en €
L’Afipa interpelle les candidats à l’élection présidentielle
« Le défi de l’industrie pharmaceutique aujourd’hui est donc de démontrer que le selfcare constitue une réponse adaptée aux nouvelles aspirations des Français et une solution durable pour maintenir le financement solidaire des affections lourdes et/ou de longue durée. En effet, le développement de l’automédication permettrait de dégager 1,5 milliard d’euros d’économies en un an », estime ainsi l’Afipa.
En mars 2016, l’association avait émis plusieurs propositions dans son manifeste visant à développer l’automédication. Les mesures s’articulaient autour de trois piliers : développer l’offre disponible en automédication en définissant une liste de pathologies bénignes et en délistant davantage de molécules ; informer et former les patients via des campagnes d’information publiques et associer les professionnels de santé à cette réforme et assurer à tous l’accessibilité financière en intégrant les dépenses d’automédication à la CMU/C et en appliquant un taux de TVA adapté à 2,1%.
C’est pourquoi dans le contexte des prochaines élections présidentielles, l’Afipa souhaite rentrer en campagne afin d’interpeller les candidats pour une réelle prise en compte du selfcare dans les programmes politiques. Le 13 février, lancera ainsi une grande opération de communication et une revendication « Selfcare et automédication ne sont pas des gros maux ».
* Réalisé auprès du panel Xpr-SO® de la société OpenHealth, panel de 3 004 pharmacies représentatives du parc officinal français. Résultats en France métropolitaine hors Corse. Les données excluent les ventes sur ordonnance. Indicateurs réalisés à partir des ventes en automédication sur le conseil du pharmacien.
Source : Afipa
