Le top 10 des médicaments les plus prescrits en officine et à l’hôpital
 Selon l’Assurance maladie, les remboursements de médicaments délivrés en officine et en rétrocession hospitalière ont enregistré une hausse de +3,8% en 2014, représentant 23 Mds € contre 22,1 Mds € en 2013.
Selon l’Assurance maladie, les remboursements de médicaments délivrés en officine et en rétrocession hospitalière ont enregistré une hausse de +3,8% en 2014, représentant 23 Mds € contre 22,1 Mds € en 2013.
Alors que les dépenses de médicaments s’étaient stabilisées en 2011 et avaient reculé en 2012 comme en 2013, l’année 2014 marque un retour à la croissance de ces dernières (+3,8%). Selon la Cnamts, il s’agit d’une « année de rupture » qui ne témoigne cependant pas d’une dérive de la prescription. En effet, cette croissance résulte exclusivement de l’arrivée sur le marché de nouveaux produits innovants dans le traitement de l’hépatite C (Sovaldi®, Daklinza®…)., « dont l’impact financier majeur explique cette inversion de tendance. »
Les 10 médicaments les plus prescrits en montants (délivrés en officine)

Les 10 premiers médicaments remboursés totalisent 2,65 Mds € de remboursements. Ce résultat évolue légèrement à la baisse depuis 2013 (2,80 Mds €). De manière globale, le classement des 5 premiers médicaments remboursés en 2014 est assez similaire à celui des deux années précédentes, avec des montants remboursés qui diffèrent néanmoins.
C’est l’Humira®, un anti-rhumatismal, qui est désormais le 1er médicament de ville remboursé avec 395 M€ de dépenses (2ème rang l’année précédente).
Lucentis®, 1er médicament de ville remboursé en 2013, passe désormais au 4ème rang en 2014 (318.2 M€). C’est la plus forte baisse des remboursements en 2014. Médicament indiqué dans la dégénérescence maculaire liée à l’âge (DMLA), il a vu son prix baisser de manière importante, en 5 étapes (juillet 2012, février 2013, mai 2014, juillet 2014 et avril 2015). En outre, l’arrivée sur le marché en novembre 2013 d’Eylea® a également joué un rôle majeur dans la baisse des montants remboursés pour cette molécule (report des prescriptions).
Doliprane (3ème rang) enregistre une nouvelle hausse de ses dépenses (320,9 M€ contre 295,4 M€ en 2013). Le principal facteur explicatif de cette dynamique est le contexte épidémique hivernal, particulièrement virulent en 2014.
Les 10 médicaments les plus prescrits en montants (rétrocession hospitalière)
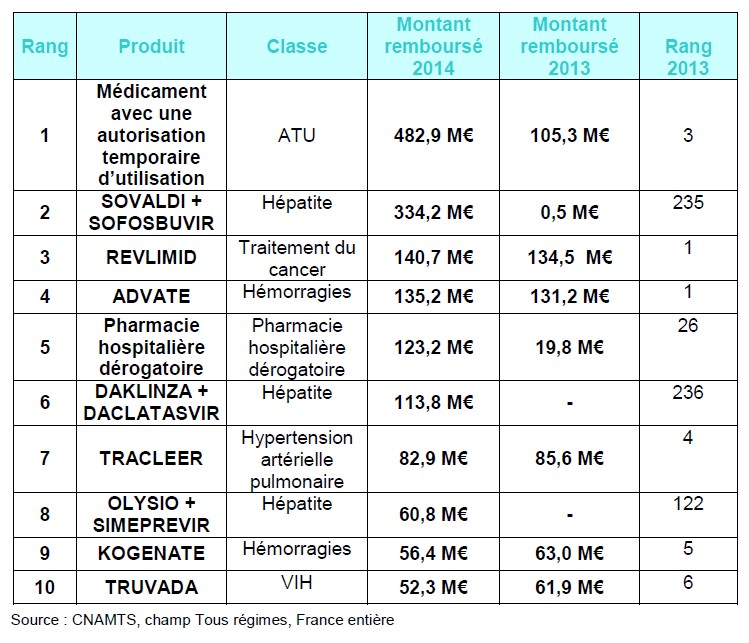
En ce qui concerne les médicaments prescrits dans le cadre de la rétrocession hospitalière, les 10 premiers médicaments remboursés totalisent 1,50 mds € de remboursements.
L’année 2014 est singulière car très fortement marquée par l’arrivée sur le marché de nouveaux produits innovants dans le traitement de l’hépatite C. Ceux-ci impactent les dépenses au travers des différents mécanismes de prise en charge. Ainsi, les dépenses liées aux traitements hépatiques sont de 514 M€ (soit +503 M€ en 2014 par rapport à 2013). Les dépenses liées à la prise en charge en ATU s’élèvent à 483 M€ (soit 378 M€ de plus par rapport à 2013). La prise en charge dérogatoire de la pharmacie hospitalière génère, quant à elle, 123 M€ de dépenses en 2014 (soit 103 M€ en plus par rapport à 2013).
Par conséquent, les premiers produits en termes de hausse des dépenses rétrocédées (hors ATU et prise en charge dérogatoire de la pharmacie hospitalière) sont Sovaldi® (Sofosbuvir, +334 M€ en 2014), Daklinza® (Daclatasvir, +114 M€) et Olysio® (Siméprévir, +61M€).
Source : Assurance maladie
