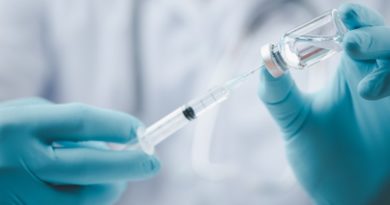
Sanofi Pasteur et Immune Design collaborent pour développer un vaccin contre Herpes simplex
 Sanofi Pasteur, la division vaccins de Sanofi et Immune Design, société de stade clinique qui développe des produits d’immunothérapie, ont annoncé jeudi le début d’une collaboration étendue pour le développement d’une thérapie immunitaire contre le virus Herpes simplex (HSV). Les deux sociétés vont développer le produit conjointement tout au long de la phase II.
Sanofi Pasteur, la division vaccins de Sanofi et Immune Design, société de stade clinique qui développe des produits d’immunothérapie, ont annoncé jeudi le début d’une collaboration étendue pour le développement d’une thérapie immunitaire contre le virus Herpes simplex (HSV). Les deux sociétés vont développer le produit conjointement tout au long de la phase II.
Dans le cadre de cette collaboration, Sanofi Pasteur et Immune Design, vont apporter chacune des produits candidats : Sanofi Pasteur va fournir HSV-529, candidat vaccin contre le HSV défectif pour la réplication, actuellement au stade clinique de développement, et Immune Design fournira G103, son candidat vaccin trivalent au stade préclinique. Les deux sociétés vont explorer en collaboration le potentiel de diverses combinaisons vaccinales, dont la plateforme GLAASTM d’Immune Design, avec l’objectif de sélectionner la meilleure thérapie immunitaire potentielle pour les patients.
« Nous avons l’intention de développer le meilleur des vaccins thérapeutiques en mettant en commun des actifs de Sanofi Pasteur et d’Immune Design », a expliqué John Shiver, docteur ès sciences, Senior Vice-Président Recherche et Développement chez Sanofi Pasteur. Et d’ajouter : « Etant donné les défis que pose le développement de vaccins, il est important d’établir des collaborations pour pouvoir répondre au besoin médical. »
Les deux sociétés vont conjointement développer les produits et les tester dans des essais cliniques de phase II, après quoi Sanofi Pasteur a l’intention de continuer le développement du candidat le plus prometteur et sera responsable de sa commercialisation. Sanofi Pasteur supportera les coûts du développement préclinique et clinique, tandis qu’Immune Design fournira à ses frais une formulation particulière de GLA issue de la plateforme GLAAS pour les essais de phase II. Immune Design pourra recevoir par la suite des paiements d’étapes et des royalties pour les produits issus de la collaboration ; les autres conditions financières de l’accord n’ont pas été rendues publiques.
Source : Sanofi Pasteur