Hypercholestérolémie familiale: Sanofi lance une campagne d’information
 Sanofi lance une campagne nationale de sensibilisation à l’hypercholestérolémie familiale qui débute à partir du 15 avril avec la mise en ligne du site web aucoeurducholesterol.fr. Menée conjointement avec les associations de patients ANHET.F et Alliance du Coeur, elle a pour objectif de sensibiliser le grand public et les professionnels de santé à cette maladie silencieuse peu connue en France.
Sanofi lance une campagne nationale de sensibilisation à l’hypercholestérolémie familiale qui débute à partir du 15 avril avec la mise en ligne du site web aucoeurducholesterol.fr. Menée conjointement avec les associations de patients ANHET.F et Alliance du Coeur, elle a pour objectif de sensibiliser le grand public et les professionnels de santé à cette maladie silencieuse peu connue en France.
Développé par Sanofi, le site www.aucoeurducholesterol.fr est une plateforme d’information et d’accompagnement des patients à haut risque cardiovasculaire et dont le taux de LDL-C est élevé. Ce site propose une section entièrement dédiée à l’hypercholestérolémie familiale, et qui permettra au grand public, concerné ou pas, d’accéder facilement à des informations sur l’hypercholestérolémie familiale, sur ses conséquences, son diagnostic ainsi que sur l’importance du dépistage familial en cascade.
Cette campagne se déclinera également sur différents supports : presse, campagne d’affichage dans les salles d’attentes des cabinets médicaux et des laboratoires d’analyses mais également sur les canaux digitaux. Par ailleurs, des vidéos d’experts et des témoignages de patients seront mis en ligne sur la chaine Youtube de Sanofi France. Un film, Heartfelt, relatant, à travers le monde, des histoires de vie de patients atteints d’un taux de LDL-élevé, sera aussi mis en ligne.
« A la différence de l’hypercholestérolémie « commune », la forme familiale est héréditaire. Sa principale caractéristique est la présence d’un taux élevé de « mauvais » cholestérol (LDL-C) dès la naissance.
Deux signes prédictifs peuvent alerter. Un taux de LDL-C supérieur à 1,9 g/L1 et des antécédents d’accidents cardiovasculaires à un jeune âge, personnels ou familiaux », indique le laboratoire dans un communiqué.
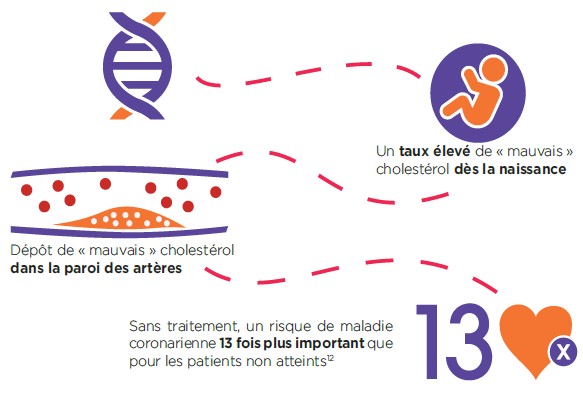
Sans traitement, le risque de maladie coronarienne est 13 fois plus important que pour les personnes non atteints. Les patients souffrant d’hypercholestérolémie familiale non traités ont 13 fois plus de risque de développer une maladie coronarienne que les personnes non atteintes. Pourtant, environ 9 malades sur 10 ne sont pas diagnostiqués. En France, jusqu’à 1 personne sur 200 pourrait présenter une hypercholestérolémie familiale.
Découvrir le site www.aucoeurducholesterol.fr