PLFSS 2016 : un déficit sous la barre des 10 milliards d’euros
 Marisol Touraine, la ministre des Affaires sociales, de la Santé et des Droits des femmes, et Christian Eckert, le secrétaire d’Etat chargé du Budget, ont présenté jeudi le projet de loi de financement de la sécurité sociale (PLFSS) pour 2016. Objectif du gouvernement : ramener son déficit en-dessous de 10 milliards d’euros. Les économies reposent sur « quatre axes structurants » : éviter les actes inutiles, baisser le prix des médicaments et développer les génériques, maîtriser les dépenses hospitalière et poursuivre le « virage ambulatoire ».
Marisol Touraine, la ministre des Affaires sociales, de la Santé et des Droits des femmes, et Christian Eckert, le secrétaire d’Etat chargé du Budget, ont présenté jeudi le projet de loi de financement de la sécurité sociale (PLFSS) pour 2016. Objectif du gouvernement : ramener son déficit en-dessous de 10 milliards d’euros. Les économies reposent sur « quatre axes structurants » : éviter les actes inutiles, baisser le prix des médicaments et développer les génériques, maîtriser les dépenses hospitalière et poursuivre le « virage ambulatoire ».
« Nous devrions ramener le déficit du régime général et du FSV sous la barre des 10 milliards d’euros. La CNAV devrait revenir à l’équilibre, pour la première fois depuis 2005. En 2016, le déficit de l’Assurance maladie sera d’environ 6 milliards d’euros. C’est 2,6 milliards de moins qu’en 2011. », a indiqué Marisol Touraine. Pour y parvenir, le gouvernement a défini une progression de l’ONDAM de 1,75%. Soit « un effort de 3,4 milliards d’euros, contre 3,2 milliards en 2015 ».
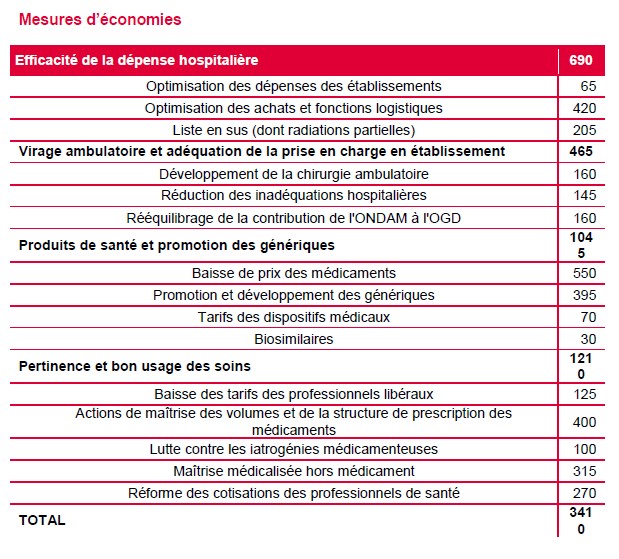
Les économies présentées jeudi reposent sur « quatre axes structurants ». Tout d’abord, le gouvernement souhaite lutter contre le gaspillage et éviter les actes inutiles ou redondants en s’appuyant sur les actions de maîtrise médicalisée de l’assurance maladie auprès des professionnels de santé. Parmi les pistes évoquées par la ministre : les examens pré-anesthésiques, les examens biologiques et le recours aux transports sanitaires. Près d’1,2 milliards d’euros d’économies sont attendus à ce titre en 2016.
Baisse des prix des produits de santé et développement des génériques
Sur les baisses de prix et le développement des génériques, le gouvernement attend 1 milliard d’euros d’économies en 2016, un niveau proche des économies réalisées l’an dernier. « Faire baisser les prix des médicaments, ce n’est pas seulement un objectif budgétaire, il s’agit aussi de financer l’innovation. », a indiqué la ministre qui a pris à titre d’exemple le traitement de l’hépatite C et des innovations en oncologie « L’an dernier, nous avons adopté des dispositifs de régulation des prix pour ces traitements coûteux : la clause de sauvegarde permanente, le taux L, et le mécanisme de régulation spécifique aux traitements de l’hépatite C. Ces dispositifs seront reconduits en 2016 », a-t-elle annoncé.
Le gouvernement maintient également son engagement de stabiliser les dépenses de médicaments remboursés entre 2015 et 2017 en poursuivant le recours aux génériques. Les médecins, en ville comme à l’hôpital, seront davantage incités à les prescrire et une grande campagne de communication sera lancée dans le courant du premier semestre 2016 pour sensibiliser les Français.
 « Garantir une médecine de proximité »
« Garantir une médecine de proximité »
Le projet de loi de modernisation du système de santé prévoit, avec les groupements hospitaliers de territoires, de doter les hôpitaux d’outils nouveaux pour accompagner ces évolutions. 700 millions d’euros sont attendus à ce titre en 2016, contre 500 millions d’euros l’an dernier. La ministre a annoncé que l’évolution de l’ONDAM hospitalier sera en ligne avec l’évolution de l’ONDAM général, à 1,75%.
Enfin, concernant le dernier axe du son projet de loi de financement de la sécurité sociale pour 2016, de nouvelles mesures viseront à « renforcer les actions entreprises pour garantir une médecine de proximité et contribuer au « virage ambulatoire ». Le gouvernement prévoit 500 millions d’euros d’économies liées au virage ambulatoire 2016. C’est un peu plus que les 400 millions d’euros réalisés en 2015. « Nous allons poursuivre cette transformation de notre système de santé, en continuant à soutenir les soins de ville. En termes comptables, la progression de l’objectif de dépense pour les soins de ville s’établira à 1,7%, mais ce chiffre tient compte de la baisse du taux de cotisation maladie des praticiens et auxiliaires médicaux. », a indiqué la ministre.
Le gouvernement souhaite par ailleurs renforcer l’accès aux soins. La réforme de « la protection universelle maladie » visera à simplifier les démarches des assurés pour faire valoir leurs droits à remboursement. Des contrats de complémentaires santé « moins chers, labellisés » pour les personnes de plus de 65 ans vont être également mise en place. Des aides financières des employeurs seront par ailleurs proposées aux salariés enchaînant les contrats très courts. Le PLFSS 2016 prévoit enfin de renforcer l’accès des mineures à la contraception et de développer la prévention de l’obésité développée chez les enfants.
Source : Ministère des Affaires sociales, de la Santé et des Droits des femmes
